一般情況下,,藥物臨床試驗(yàn)的審批時(shí)間相對(duì)較長。如今,,面對(duì)新發(fā),、突發(fā)疫情,在不降低標(biāo)準(zhǔn)的情況下,,各項(xiàng)審批流程都在加快,,這對(duì)患者來說是極大的利好消息。但是,,研發(fā)臨床藥物和確定診療方案有其特定的科學(xué)規(guī)律,不可亂來,。尤其在一線臨床工作量極大,、醫(yī)護(hù)人手非常緊張的情況下,既要鼓勵(lì)創(chuàng)新,,也要防止心浮氣躁,、急于冒進(jìn)。
近日,,記者用“新型冠狀病毒肺炎”等關(guān)鍵詞,,在中國臨床試驗(yàn)注冊中心查詢發(fā)現(xiàn),截至2月12日已有60項(xiàng)符合檢索條件的試驗(yàn),。這些臨床試驗(yàn)內(nèi)容非常廣泛,,既包括多種西藥、干細(xì)胞,、中藥,、重要注射劑,,還包括社區(qū)干預(yù)療法等。令記者沒想到的是,,其中竟然還有一項(xiàng)預(yù)注冊方案,,準(zhǔn)備研究太極拳對(duì)患者康復(fù)期肺功能及生存質(zhì)量的影響。
在當(dāng)前公開輿論中,,已多次出現(xiàn)各種吹噓“神醫(yī)薦藥”的文章,,常常有“因?yàn)楹攘诉@例藥湯,500多人都沒有感染”之類的標(biāo)題,。事實(shí)上,,這種“民間偏方”,既無法排除一些疾病是自限性疾病,、患者自行痊愈了的情況,,又無法研究藥物的副作用,如果盲信,、盲從會(huì)耽誤診療,。
無論什么藥物,最終都要用在病人身上,,安全性和有效性是最必要的前提,。臨床藥物研發(fā)之所以要分一期、二期,、三期試驗(yàn),,就是要在不同試驗(yàn)進(jìn)程中,通過雙盲,、隨機(jī)等安排,,驗(yàn)證其安全性和有效性。是否有毒副作用,、會(huì)不會(huì)留下后遺癥,,都需要數(shù)據(jù)說話。新冠病毒是人類歷史上首次遭遇的病毒,,和它“交戰(zhàn)”既不能輕視,,又不能武斷。
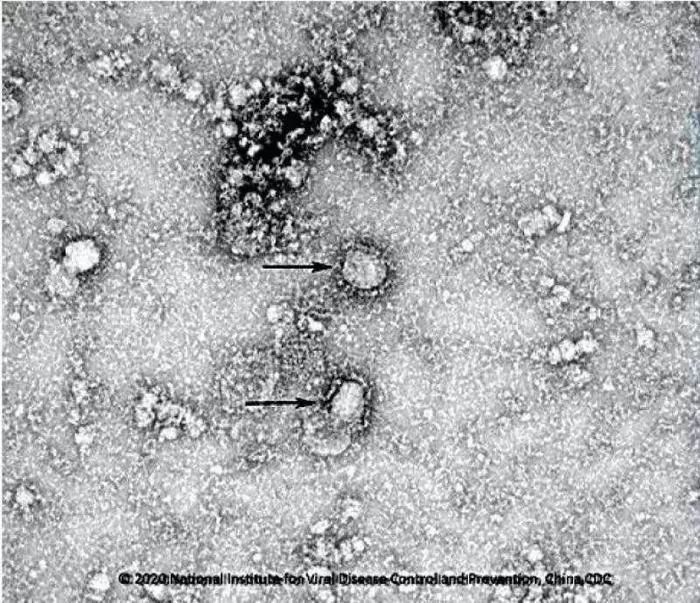
資料圖:新型冠狀病毒武漢株01 圖片來源:中國疾控中心網(wǎng)
從體外細(xì)胞水平試驗(yàn)到動(dòng)物實(shí)驗(yàn),,再到人體試驗(yàn),,藥物研發(fā)是逐步推進(jìn)的過程。當(dāng)前,,不少藥物還處在體外細(xì)胞水平的階段,,這離最終臨床被證實(shí)有效、能對(duì)癥治療,,還有很長一段路要走,。例如,,體外細(xì)胞試驗(yàn)往往需要極高濃度的藥物,按照這一高濃度用于病人臨床,,有時(shí)副作用可能遠(yuǎn)高于療效,。
臨床試驗(yàn)用于檢驗(yàn)藥物,在現(xiàn)在情況下,,也并非多多益善,。每檢測一種藥物,都需要耗費(fèi)多種資源,。尤其在臨床工作量極大背景下,,開展過多的新藥臨床研究,還會(huì)占用臨床醫(yī)護(hù)人員的大量精力,。越是在緊急的情況下,,走到臨床試驗(yàn)的方案越要能給出足夠的邏輯和依據(jù),不能隨意降低標(biāo)準(zhǔn),,更不能“病急亂投醫(yī),、亂用藥”。
疫情當(dāng)前,,一些人產(chǎn)生“神藥”期待心理,,這可以理解。但如果因此就對(duì)一些還在研究中的藥物自行服用,,必然暗藏隱患,。總之,,對(duì)于一個(gè)新發(fā)現(xiàn)的病毒,,現(xiàn)在定義任何藥有特別確切的作用,可能都為時(shí)過早,。針對(duì)這點(diǎn),,更需要科研院所、媒體,、政府部門等在信息發(fā)布時(shí)保持審慎,,尊重科學(xué)規(guī)律,、注重實(shí)事求是,,避免夸大、拔高,,做好科普,。(評(píng)論員 周琳)


